人體試驗的結果令人震驚。一位病人僅僅靜脈注射了兩小時的一種實驗性抗癌藥物,劑量較平時還要小,體內的雙肺多發轉移瘤就開始縮小,有的甚至消失不見。另一位病人接受了 6 個月治療后,體內的宮頸瘤縮小了近 60%。此次由位于美國馬薩諸塞州劍橋市的生物科學公司 bindbiosciences 設計的藥物試驗,只是為了證明這項基于納米技術的實驗性療法是否安全。但是,令人倍受鼓舞的試驗結果再一次點燃了人們對于納米藥物的希望。
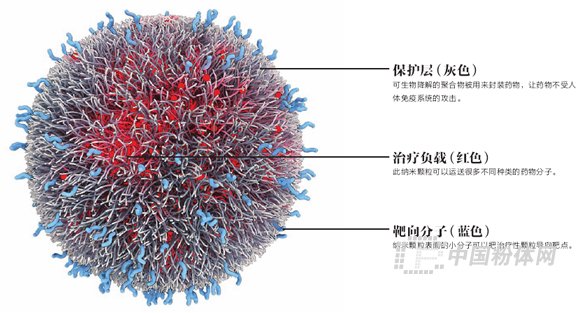
十多年來,研究人員一直在努力研發能更有效、更安全地投遞藥物的納米顆粒。他們的研究目標是讓攜帶藥物化合物的納米顆粒有選擇性地瞄準腫瘤細胞或其他病變細胞,同時避開健康的細胞。納米微粒的表面可附著抗體或其他分子,以精確識別靶向細胞。美國國立癌癥研究所納米技術研發項目的負責人薩拉·胡克(Sara Hook)表示:“納米科技的最大優勢之一,就是可以對粒子形式的東西進行改造,這樣就能專門針對腫瘤細胞化療,從而保護人體的健康細胞,使患者免受副作用的不良影響。”
然而,實現這一設想的難度很大。挑戰之一是:藥物在與納米微粒結合后,藥物在人體內的藥性會發生極大的改變。納米微粒能夠改變藥物的溶解性、毒性和起效速度等——這有時是好事,有時則是壞事。如果一種藥物的主要問題在于它對于非目標組織是有毒的,那么納米技術能夠確保藥物被投遞到病變細胞而非健康細胞。而如果一種藥物需要被病變細胞快速吸收才能夠發揮功效,那么納米微粒就有可能減慢吸收過程,將一種最優治療變為次優。
成立于 2007 年的 bind 公司,致力于研制出新型靶向給藥納米微粒,系統地改變微粒的結構和成分,從而攻克上述難題。一般而言,靶向藥物納米微粒的制造過程分為兩個步驟:首先,藥物被封入一個納米顆粒中;然后,將粒子的外表面與靶向分子綁定在一起,通過靶向分子把治療性顆粒導向病變細胞。這種納米顆粒的制造過程很難控制和復制,因此限制了研究人員對納米顆粒的表面屬性進行微調的能力。為了避開這一難題,bind 公司利用自組裝技術合成了攜帶藥物的納米微粒。公司技術研發部高級副總裁杰夫·哈卡克(Jeff Hrkach)表示:“為了優化每種藥物的療效,我們會進行數百次的組合測試。”

麻省理工學院羅伯特·蘭格教授團隊開發出了控制藥物釋放的納米顆粒(圖片來源:MIT)
bind 公司聯合創始人、哈佛大學醫學院 brigham 婦女醫院副教授奧米德·法羅扎德(Omid Farokhzad)曾在麻省理工學院跟隨化學工程教授羅伯特·蘭格(RobertLanger)做博士后研究員,期間他研究出了一種制造納米顆粒的新方法。蘭格的團隊當時已經開發出能夠控制藥物釋放的納米顆粒,但這些顆粒還無法辨認出癌細胞。法羅扎德面對的第一個挑戰,就是制造出能夠對癌細胞進行靶向治療的納米顆粒分子,并讓它們在血液中不顯得特殊,免遭免疫系統的消滅。第二個挑戰是,找到一種穩定、可復制的制造過程。
法羅扎德和蘭格發現了一種方法,對納米顆粒和藥物這兩個部分進行自組合,生成最終產品。兩種聚合物構成了一張復雜的納米顆粒網,顆粒上搭載著藥物。其中一種聚合物在化學和結構上分成截然不同的兩個區域,即“塊區”(block):不溶于水的塊區構成了包裹藥物的保護網的一部分,而可溶于水的塊區為最終產品披上了一件隱形外衣,可以規避免疫系統。另一種聚合物由三個塊區組成:前兩個塊區與第一種聚合物相同,第三個塊區含有一個靶向分子——確保最終顆粒附著到目標細胞上。制成攜帶藥物的納米顆粒很簡單,就是將這些聚合物以合適的比例與藥物進行混合。
這些自組合的聚合體能夠可重復地批量生產。這種方法還有一個額外的好處,這也可能是bind公司獲得成功的真正關鍵所在。這種制造納米顆粒的方法——即單獨制備具有兩個或三個塊區的聚合物,可以讓研究人員使用高通量的篩選方式。這和藥物化學家們設計和測試新藥的方式相類似。每一個塊區都可以進行微調——擴大某一塊區,改變另一塊區的藥量——并且可以改變每個聚合物的相對數量。
bind-014 是該公司第一款進行臨床試驗的藥物。該藥物攜帶一種被廣泛使用的化療藥物多西他賽(docetaxel),可通過血流到達癌細胞。藥物被封在一個由可生物降解的聚合體構成的球形納米顆粒中,這種聚合體能夠保護藥物并避開人體的免疫系統。每個納米顆粒的外表面都分布著多個能夠靶向癌細胞的分子。這些納米顆粒一旦接觸到目標細胞,就會附著在它們的表面,致使目標細胞吞沒顆粒。藥物從顆粒中有序地滲出,進入病變細胞。
加州理工學院教授馬克·戴維斯(MarkDavis)期望,正在進行臨床試驗的這些靶向納米顆粒療法,包括bind-014 以及他的實驗室中研制出的一種療法,能夠展示出這項技術的潛力。“除非(后期臨床試驗)能夠在統計學上顯著地證明這些定向納米顆粒對病人確實有效,否則醫學界根本不會產生任何興奮之情。”目前,參與 bind-014 一期臨床試驗的 17 位患者的結果看上去充滿了希望,但真正的有效性測試要等到可能在2012 年下半年開始的二期臨床試驗。
bind 公司使用的這種“可編程”設計,可能成為將更多的納米顆粒靶向藥物投入人體試驗的關鍵所在。該方法能夠應用于現有的任何一種藥物或化合物上,包括那些已經被制藥公司下架的對人全身毒性過大的藥物。“我們相信,我們將有一個十分寬廣的可開發藥物的平臺。”哈卡克說。(作者 Susan Young)

十多年來,研究人員一直在努力研發能更有效、更安全地投遞藥物的納米顆粒。他們的研究目標是讓攜帶藥物化合物的納米顆粒有選擇性地瞄準腫瘤細胞或其他病變細胞,同時避開健康的細胞。納米微粒的表面可附著抗體或其他分子,以精確識別靶向細胞。美國國立癌癥研究所納米技術研發項目的負責人薩拉·胡克(Sara Hook)表示:“納米科技的最大優勢之一,就是可以對粒子形式的東西進行改造,這樣就能專門針對腫瘤細胞化療,從而保護人體的健康細胞,使患者免受副作用的不良影響。”
然而,實現這一設想的難度很大。挑戰之一是:藥物在與納米微粒結合后,藥物在人體內的藥性會發生極大的改變。納米微粒能夠改變藥物的溶解性、毒性和起效速度等——這有時是好事,有時則是壞事。如果一種藥物的主要問題在于它對于非目標組織是有毒的,那么納米技術能夠確保藥物被投遞到病變細胞而非健康細胞。而如果一種藥物需要被病變細胞快速吸收才能夠發揮功效,那么納米微粒就有可能減慢吸收過程,將一種最優治療變為次優。
成立于 2007 年的 bind 公司,致力于研制出新型靶向給藥納米微粒,系統地改變微粒的結構和成分,從而攻克上述難題。一般而言,靶向藥物納米微粒的制造過程分為兩個步驟:首先,藥物被封入一個納米顆粒中;然后,將粒子的外表面與靶向分子綁定在一起,通過靶向分子把治療性顆粒導向病變細胞。這種納米顆粒的制造過程很難控制和復制,因此限制了研究人員對納米顆粒的表面屬性進行微調的能力。為了避開這一難題,bind 公司利用自組裝技術合成了攜帶藥物的納米微粒。公司技術研發部高級副總裁杰夫·哈卡克(Jeff Hrkach)表示:“為了優化每種藥物的療效,我們會進行數百次的組合測試。”

麻省理工學院羅伯特·蘭格教授團隊開發出了控制藥物釋放的納米顆粒(圖片來源:MIT)
bind 公司聯合創始人、哈佛大學醫學院 brigham 婦女醫院副教授奧米德·法羅扎德(Omid Farokhzad)曾在麻省理工學院跟隨化學工程教授羅伯特·蘭格(RobertLanger)做博士后研究員,期間他研究出了一種制造納米顆粒的新方法。蘭格的團隊當時已經開發出能夠控制藥物釋放的納米顆粒,但這些顆粒還無法辨認出癌細胞。法羅扎德面對的第一個挑戰,就是制造出能夠對癌細胞進行靶向治療的納米顆粒分子,并讓它們在血液中不顯得特殊,免遭免疫系統的消滅。第二個挑戰是,找到一種穩定、可復制的制造過程。
法羅扎德和蘭格發現了一種方法,對納米顆粒和藥物這兩個部分進行自組合,生成最終產品。兩種聚合物構成了一張復雜的納米顆粒網,顆粒上搭載著藥物。其中一種聚合物在化學和結構上分成截然不同的兩個區域,即“塊區”(block):不溶于水的塊區構成了包裹藥物的保護網的一部分,而可溶于水的塊區為最終產品披上了一件隱形外衣,可以規避免疫系統。另一種聚合物由三個塊區組成:前兩個塊區與第一種聚合物相同,第三個塊區含有一個靶向分子——確保最終顆粒附著到目標細胞上。制成攜帶藥物的納米顆粒很簡單,就是將這些聚合物以合適的比例與藥物進行混合。
這些自組合的聚合體能夠可重復地批量生產。這種方法還有一個額外的好處,這也可能是bind公司獲得成功的真正關鍵所在。這種制造納米顆粒的方法——即單獨制備具有兩個或三個塊區的聚合物,可以讓研究人員使用高通量的篩選方式。這和藥物化學家們設計和測試新藥的方式相類似。每一個塊區都可以進行微調——擴大某一塊區,改變另一塊區的藥量——并且可以改變每個聚合物的相對數量。
bind-014 是該公司第一款進行臨床試驗的藥物。該藥物攜帶一種被廣泛使用的化療藥物多西他賽(docetaxel),可通過血流到達癌細胞。藥物被封在一個由可生物降解的聚合體構成的球形納米顆粒中,這種聚合體能夠保護藥物并避開人體的免疫系統。每個納米顆粒的外表面都分布著多個能夠靶向癌細胞的分子。這些納米顆粒一旦接觸到目標細胞,就會附著在它們的表面,致使目標細胞吞沒顆粒。藥物從顆粒中有序地滲出,進入病變細胞。
加州理工學院教授馬克·戴維斯(MarkDavis)期望,正在進行臨床試驗的這些靶向納米顆粒療法,包括bind-014 以及他的實驗室中研制出的一種療法,能夠展示出這項技術的潛力。“除非(后期臨床試驗)能夠在統計學上顯著地證明這些定向納米顆粒對病人確實有效,否則醫學界根本不會產生任何興奮之情。”目前,參與 bind-014 一期臨床試驗的 17 位患者的結果看上去充滿了希望,但真正的有效性測試要等到可能在2012 年下半年開始的二期臨床試驗。
bind 公司使用的這種“可編程”設計,可能成為將更多的納米顆粒靶向藥物投入人體試驗的關鍵所在。該方法能夠應用于現有的任何一種藥物或化合物上,包括那些已經被制藥公司下架的對人全身毒性過大的藥物。“我們相信,我們將有一個十分寬廣的可開發藥物的平臺。”哈卡克說。(作者 Susan Young)