中國粉體網訊: 可能許多人都曾思考過,藥怎么能治病的問題,如:藥物怎么知道我哪里病了?它是怎么過去的?它在病灶那里停下?過去之后它是不是沒多少效果了?或許后來隨著知識的增加知道腸道吸收和血液循環輸送等,但是遠遠不能解答我們的疑問。今天,我們一起來全面了解一下藥物傳遞這個領域中的新貴,介孔二氧化硅,看看這位體內的藥物快遞小哥是怎么工作的,它如何形成藥物傳遞系統,又有怎樣的表現,也順便找一下前面小問題的答案。
孔二氧化硅納米顆粒(Mesoporous Silica Nanoparticles,MSNs)是一種重要的形態優越、骨架穩定、強度出色的多孔材料。其具有良好生物相容性、有序介孔結構、比表面積大、表面易修飾性、光致發光性能等特點,在很多生物醫藥領域顯示出了極大的應用前景,尤其是基于MSNs的納米藥物輸送體系被廣泛用于各種藥物的遞送。
本文將對其當前研究進展、結構特點、合成方法和種類進行介紹。并重點展開講述不同結構的介孔二氧化硅藥物傳遞系統,不同刺激響應性的藥物遞送系統,以及藥物遞送效率的影響因素等多點內容。希望,與大家一起了解介孔二氧化硅在醫藥領域的廣泛應用和巨大潛力。
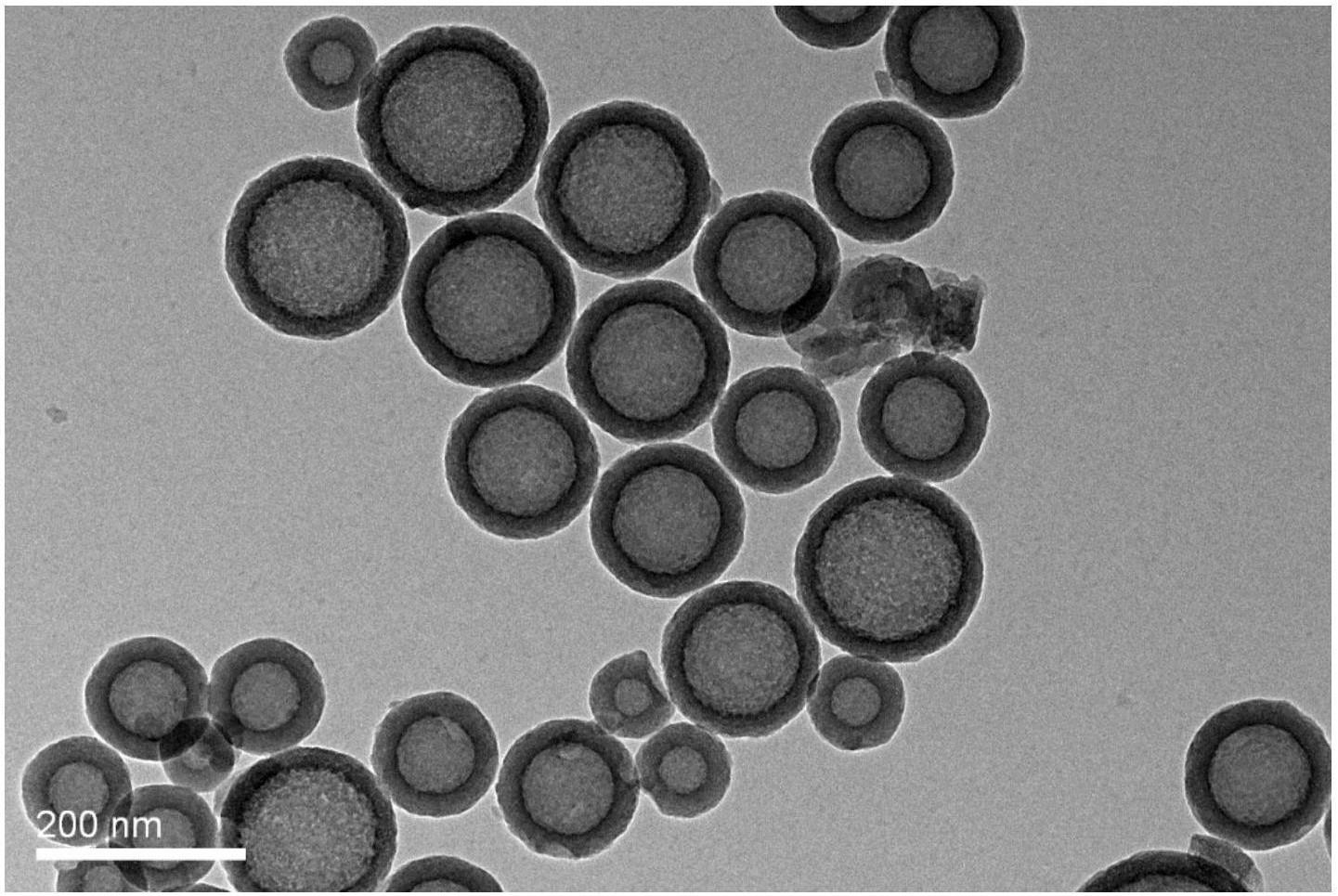
中空介孔二氧化硅的TEM圖
一、 MSNs的研究進展
納米制劑與常規藥物相比,具有增加藥物溶解度、提高藥物穩定性、緩釋控釋藥物等多方面優勢。介孔二氧化硅因多孔性、比表面積大、便于修飾性、毒性低等特點,得到廣泛應用,具有極大的開發前景,但是介孔二氧化硅的載藥容積有限,在生物體內代謝慢,裝載的藥物容易泄漏。科學家在MSNs的基礎上進一步擴展,制備出中空介孔二氧化硅納米粒(HMSNs)。HMSNs的空腔與介孔結構極大地增大了載藥容積,藥物裝載量得到了有效提升,更可貴的是,中空介孔二氧化硅特殊的雙層結構能實現親疏水性兩種不同性質的藥物的共包封,為藥物的聯合治療提供了新思路。隨后出現的膜包被技術使科研工作者能夠在阻止藥物泄漏等問題上進行多種有益嘗試。
上世紀90年代,MSN被廣泛應用于分子篩。2001年,Vallet-Regi等首先將MCM-41(介孔二氧化硅的一種)用作藥物載體在藥物傳遞系統中應用。此后,對介孔材料在生物醫藥學的研究有了顯著的增加。除了MCM-41,其他結構的介孔二氧化硅材料如SBA-15和MCM-48也被作為載體用于藥物傳遞系統的研究。SBA-15的孔徑大約在4~10nm的范圍內,而MCM-41的孔徑比較小,一般在2~4nm的范圍內。MSN具有巨大的比表面積、可調的介孔孔徑、結構穩定、易于修飾、生物相容性好等一系列優點成為理想的藥物載體材料。
二、 MSNs的結構特點
介孔二氧化硅材料的主要特征是具有規則的多孔結構,孔徑均勻排列,并且孔徑之間彼此獨立,同時具有很高的比表面積(>900m2/g)和孔容積(>0.9cm'/g)以及較高的熱穩定性,其孔徑大小也可以從幾納米到十幾納米范圍內進行控制。由于介孔二氧化硅材料含有許多硅羥基,所以可以對其表面和介孔孔道進行不同官能團的修飾,以擴大其應用范圍。
三、MSNs的合成
1、制備方法介紹:
當前的介孔二氧化硅材料的合成方法主要是基于使用表面活性劑作為結構導向劑,合成方法包括溶膠-凝膠法、水熱合成法、微波合成法、模板合成法、改進的氣凝膠法、快速自組裝等。其中,基于溶膠-凝膠法的模板合成法因其反應條件溫和、操作便利成為了目前最為常用的方法。其根據模板的種類和原理又可分為軟模板法和硬模板法。
2、可降解MSNs與其制備方法
另外,一般的MSNs不易被代謝,研究發現MSNs在體內需要4周才能被清除完全,機體若來不及將其代謝完全,容易在肝和脾內過多堆積,對組織器官造成一定損傷。可降解的MSNs作為新穎且前景光明的載藥工具應運而生。Shen等制備的可降解的MSNs在遞送藥物后,在體內一段時間內能夠被快速清除,避免了納米粒在體內的過多堆積造成組織器官的損傷。而且,其制備方法也相當新穎:以十六烷基三甲基氯化銨(CTAC)為模版膠束,TEOS環己烷溶液在油水界面(油相在上,水相在下)水解形成MSNs,再用硝酸銨乙醇溶液萃取除掉CTAC即得。
可降解的MSNs在模擬生理條件的Krebs溶液中會隨著時間的延長而逐漸從外向內降解,在4d后,MSNs納米粒消失,降解完全。可降解的MSNs在制備過程中可以通過控制反應時間來控制納米粒的尺寸,調節TEOS的量或油相的種類來調節孔徑的大小。可降解的MSNs不僅材料尺寸、孔徑可調,其獨特的可降解性進一步優化了載體,使其在疾病的診斷與治療方面得到更好的應用。
四、 介孔二氧化硅藥物遞送系統
鑒于介孔二氧化硅制備方式和結構的不同,出現了不同結構的介孔二氧化硅藥物遞送系統。在實際應用中,鑒于藥理、病理的不同,可以根據多方特點靈活選擇。
1、 MCM結構的介孔二氧化硅
MCM是mobil composition of matter的簡稱。MCM系列的介孔二氧化硅主要是美孚石油公司以硅酸乙酯為硅源通過膠束軟模板法合成。在MCM系列中,針對MCM-41的研究最為普遍。MCM-41具有由規整的圓柱形介孔排列而成的一維孔道結構孔徑可以在2.0~6.5nm之間調節。正是由于具有這種有序可控的孔道結構,MCM-41可以使藥物均勻地裝載并實現藥物的有效遞送。
Qu等利用MCM-41系統作為水溶性藥物卡托普利的載體,發現其可以使藥物緩慢可控地釋放。Mathew等利用N-[3(三甲氧基硅基)丙基]苯胺和苯基三甲氧基硅烷修飾的MCM-41來用作難溶性藥物的載體。Rakhshaei等將摻入氧化鋅的MCM-41作為藥物載體,并與羧甲基纖維素水凝膠組合制備形成了柔性納米復合水凝膠膜再用四環素研究了納米復合水凝膠膜的藥物遞送性能,結果顯示四環素可以持續可控地釋放。
MCM-48是MCM體系中另一類重要的介孔二氧化硅材料。與MCM-41的單向孔道不同,MCM-48具有兩套相互獨立的三維立方螺旋孔道網絡結構,因而具有比MCM-41更高的吸附動力學參數,且傳質更快。
2、 SBA結構的介孔二氧化硅
SBA是santa barbara amorphous的簡稱。SBA系列的介孔二氧化硅是利用嵌段型表面活性劑通過軟模板法來合成,具有高度有序的六邊形結構,孔徑在5~ 30nm范圍內可調。其中,研究較為廣泛的是SBA-15。由于其孔壁較厚,相對于MCM系列材料來說,SBA-15的水熱穩定性更好,且SBA-15的孔徑通常大于MCM-41的孔徑這對藥物分子體積的限制作用會更小。
Wang等分別用SBA-15以及氨丙基修飾的SBA-15作為黃芩苷的藥物載體其中藥物的負載量分別為36.3%和39.1%(質量分數),藥物的釋放量則分別為72.2%和98.4%。類似地,Eren等用氨丙基修飾的SBA-15以及硼摻雜的SBA-15作為難溶性藥物塞來昔布的載體,結果表明:前者可以使藥物緩慢可控地釋放,而后者則表現為突釋。這均揭示了藥物釋放行為高度依賴于SBA-15不同的表面性質。近期Cussa等利用SBA-15作為鎮痛藥酮咯酸氨丁三醇的藥物載體,顯著改善了該藥的控制釋放行為并增強了鎮痛效果。
3、HMS結構的介孔二氧化硅
HMS,一種中空介孔材料。HMS可以通過軟模板法或硬模板法來合成其具有可調的孔徑和中空空隙。與傳統的介孔材料相比,其在藥物遞送和擴散方面表現出更多的優勢。
Zhu等報道了利用HMS作為布洛芬的藥物載體。將HMS的藥物吸附量與MCM-41進行比較,結果表明,HMS具有比MCM-41更大的藥物吸附量。進一步使用阿司匹林作為模型藥物研究結果也表明,由于HMS具有較高的比表面積和中空結構在HMS中阿司匹林的吸附量高于常規的MCM-48和MCM-41。同時,他們發現HMS、MCM-48和MCM-41作為阿司匹林的藥物遞送系統,在體外釋放過程中同樣具有持續釋放的特性,并遵循Fickian擴散機制。
Li等利用金納米顆粒和十六烷基三甲基溴化銨作為雙模板合成了一系列殼厚度可調的HMS,并將其作為多柔比星的藥物載體研究了體外釋藥行為。結果發現:通過調整殼層的厚度,可以靈活方便地控制HMS中藥物的釋放。Fu等和Yang等則在HMS表面修飾多種基團使其成為多功能智能響應性藥物載體。
如上所述,由于可控的孔徑、高的比表面積以及表面易修飾的特性,多種介孔二氧硅體系均可以作為良好的藥物遞送系統。
五、介孔二氧化硅刺激響應性藥物遞送系統
經研究,介孔二氧化硅的諸多理化特性在藥物遞送系統中被不斷挖掘和應用。其中,介孔二氧化硅對不同傳遞環境的不同刺激相應特性被重點應用,整個藥物傳遞系統也得到持續拓展,因此在臨床中面對許多疾病也都了有不同的藥物傳遞手段和治療思路。
1、pH響應性的藥物遞送系統
迄今為止,研究者已經開發出了多種pH響應性的藥物遞送系統。生物體內pH的變化主要來源于以下兩點:與正常組織相比,腫瘤部位的pH為5.8~7.6;人體整個胃腸道的pH范圍較為廣泛,胃內的pH為1.0~3.0,小腸內的pH為6.5~7.0,而結腸的pH為7.0~8.0。因此,基于酸性pH響應的藥物遞送系統可以靶向地控制藥物釋放到腫瘤部位。
Fisher等利用Al-MCM-41和熒光素作為模型首次研究了pH變化對藥物分子釋放的影響。近年來,Li等利用兩種不同功能化的β-環糊精,通過疏水相互作用與MCM-41連接,將抗菌藥物莫西沙星封裝在孔道中。當pH降低時,功能化的環糊精發生質子化解離而使藥物釋放出來。Cheng等將D-α-琥珀酸生育酚聚乙二醇酯與聚多巴胺官能化的介孔二氧化硅作為pH響應性的藥物遞送系統用于可控地遞送多柔比星來治療非小細胞肺癌。Rim等則利用可吸收的磷化鈣(CaP)包被的介孔二氧化硅作為pH響應性藥物遞送系統。當pH較低時,CaР溶解使封裝的藥物更容易地釋放出來。Li等設計合成了一種以金納米粒子為核心、碳介孔二氧化硅為外殼的中空納米膠囊,進一步將多柔比星裝載在納米膠囊中形成了復合的藥物遞送系統。由于pH的變化,藥物分子和納米膠囊間的范德華力發生改變而使藥物釋放出來。Kienzle等介紹了一種新型的樹突狀介孔二氧化硅并使其作為腫瘤壞死因子α(TNF-a)的 pH響應性遞送系統。
3、 氧化還原響應性藥物遞送系統
利用氧化還原反應介導藥物釋放是刺激響應性藥物遞送系統中的又一實例。二硫鍵易于與各種還原劑發生反應,因而具有敏感的氧化還原特性可以作為氧化還原響應性藥物遞送系統的作用位點。
Xiao等將富含色氨酸的支鏈肽通過二硫鍵與介孔二氧化硅連接而使藥物封裝在孔道中。一旦其被吞入癌細胞中胞內高濃度的谷胱甘肽會使二硫鍵斷裂,支鏈肽脫離,促使藥物從孔道中釋放出來。Wu等成功合成了一種中空介孔有機硅,并通過二硫鍵在其上連接聚β-氨基酯作為siRNA以及多柔比星的氧化還原響應性藥物遞送系統。Palanikumar等通過一鍋法合成了聚合物連接的介孔二氧化硅合成過程中添加含有硫醇的配體分子,使負載在孔道中的藥物分子可以通過胞內的還原性微環境靶向釋放。類似地Zhang等通過一鍋法合成了含有二硫鍵的介孔二氧化硅作為多柔比星的氧化還原響應性藥物遞送系統。
3、溫度響應性藥物遞送系統
在刺激響應性藥物遞送系統中除pH和氧化還原響應外另一種常見的刺激響應方式是溫度響應。其中將連接有聚N-異丙基丙烯酰胺(pNIPAM)的介孔二氧化硅作為溫度響應性復合藥物遞送系統的研究最為普遍。pNIPAM是一種理想的溫度敏感性聚合物其可以在低臨界溶解溫度(LCST)(約32℃)下完成親水性到疏水性的轉變。介孔二氧化硅與pNIPAM復合材料主要通過以下原理來實現溫度響應。首先將pNIPAM 聚合物沉積在介孔二氧化硅的孔內或表面。在LCST以下時由于pNIPAM分子鏈溶脹阻塞孔道,且pNIPAM和藥物分子間可以形成氫鍵,能夠防止藥物從孔道中釋放。在LCST之上時,聚合物轉變為疏水性并收縮,導致孔道的開放和氫鍵的斷裂,進而使藥物分子釋放出來。Ugazio等利用介孔二氧化硅與pNIPAM復合材料作為柚皮素的溫度響應性藥物遞送系統,并將其應用在皮膚病治療方面。Bathfield等則直接將pNIPAM和硅源混合,一步合成了溫度響應性的藥物遞送系統,該方法簡單又快捷。
Ruiz-Hernandez等和Schlossbauer等探索了一種新型的基于DNA熱響應性藥物遞送系統其中DNA/磁性納米顆粒和生物素標記的DNA能夠覆蓋介孔二氧化硅的孔道。在特定的DNA解鏈溫度下,DNA雙鏈打開使孔道開放,從而釋放裝載在孔中的模型藥物。
4、光響應性藥物遞送系統
光也是刺激響應性藥物遞送系統的一種刺激因素。Ferris等報道了在MCM-41中裝載偶氮苯衍生物從而開發了光響應性藥物遞送系統。偶氮苯及其衍生物在紫外-可見光下可以發生可逆性轉變。在可見光下,偶氮苯衍生物為反式結構,可以與β-環糊精結合而阻止MCM-41孔道中藥物的釋放。在300~380nm光照射下,它的結構從反式轉變為順式,而從β-環糊精上解離下來,MCM-41孔道中藥物得以釋放。因此,偶氮苯及其衍生物能夠對藥物釋放具有光響應性。
類似地Li等合成了內核為金納米粒子、外殼為碳—二氧化硅的復合納米膠囊,用以裝載多柔比星,結果表明該復合體系能夠實現藥物對NIR響應性的靶向釋放。Liu等則制備了外層連接單壁碳納米管的介孔二氧化硅作為多柔比星的NIR響應性藥物遞送系統。
5、超聲響應性藥物遞送系統
超聲波具有非侵入性、無電離輻射等優點,且可以通過調諧頻率、占空比和超聲時間來調節組織穿透深度,可作為藥物可控釋放的外部刺激因素。
在Kim等的研究工作中,他們利用聚二甲基硅氧烷-介孔二氧化硅復合材料來裝載布洛芬,使其可以在超聲刺激下釋放。Paris等開發了一種新型的溫度-超聲雙重響應性藥物遞送系統。他們將一種溫度響應性和超聲響應性的共聚物接枝在介孔二氧化硅表面上。在4℃時,溫度響應性聚合物為親水性,藥物分子可以擴散到開放的孔道中。在37℃時其則轉變為疏水性阻止藥物分子進出孔道。然而,在超聲波的作用下,超聲響應性疏水聚合物四氫吡喃甲基丙烯酸酯可以被水解為親水性的甲基丙烯酸極性的變化會引起孔道的開放進而使藥物分子釋放出來。Lv等合成了介孔二氧化硅與微泡復合材料來作為超聲響應性的藥物遞送系統。他們利用表面修飾葉酸的介孔二氧化硅裝載丹參酮IIA并將其封裝在氣體填充的微泡中在超聲波的刺激下,微泡破裂而使藥物釋放出來。
六、介孔二氧化硅載體中藥物遞送效率的影響因素
作為藥物載體,介孔二氧化硅中的藥物遞送的效率必然是研究和應用的焦點,不過其效率受載體孔徑、孔結構類型、比表面積等多方因素影響,在各種情況下有不同的遞送效率。
1、孔徑
一般情況下藥物的吸附是將高度濃縮的藥物溶液浸泡在介孔二氧化硅基質中來實現的,而該方法主要依賴于基質的吸附性能。基質的孔徑決定了可吸附到孔道中藥物分子的大小。孔徑的減小必然會導致藥物吸附量及釋放速率的降低,這與空間位阻效應相關聯。
Vallet-Regi等使用不同鏈長的表面活性劑十二烷基三甲基溴化銨(C12TAB)和十六烷基三甲基溴化銨(C16TAB)制備得到不同孔徑的MCM-41,并將其作為布洛芬的藥物載體,結果顯示:使用C16TAB獲得的具有較大孔徑的MCM-41藥物遞送系統,體外釋藥24h后約有68%的藥物被釋放出來。相比之下,用C12TAB獲得的MCM-41在同一時間段內僅釋放了55%的藥物。
同時,研究結果表明用以吸附藥物的MCM-41初始狀態不同對藥物的釋放行為也有一定的影響。進一步的研究也證實了介孔二氧化硅的孔徑是影響藥物釋放速率的關鍵因素之—。當MCM-41藥物遞送系統的孔徑在2.5~3.6nm時,藥物釋放速率會隨孔徑的增大而顯著增加。類似地,Jia等通過控制反應時間合成了3種不同孔徑的介孔二氧化硅,并將其作為紫杉醇的載體研究了藥物的體外釋放行為,發現了藥物的釋放速率依賴于孔徑的大小。
2、比表面積
大量研究已經表明,比表面積是影響親水性及多含官能團藥物分子吸附量的重要因素。具有更多硅羥基的介孔二氧化硅能夠提供更多的活性位點,從而增加了藥物吸附量。Azais等合成了BEI比表面積分別為987和775m2/g的MCM-41。兩者在相同的條件下吸附布洛芬的量分別為670和600mgl/g,這表明了藥物吸附量會隨著比表面積的增加而增加。
3、孔容
藥物與介孔的相互作用是表面吸附用,然而藥物與藥物之間的靜電相互作用可能會導致孔道的堵塞。因此,孔容亦是影響藥物吸附量的重要內素。簡而言之,孔容越大,藥物的吸附量越高。一有研究表明,孔容分別為1.18和0.28㎝3/g的MCM-41對卡托普利的吸附量可以達到33.99%和23.60%(質量分數)。因此,孔容是影響藥物吸附量的另一個重要因素。
4、孔結構類型
介孔二氧化硅的孔結構類型對藥物的吸附和釋放也有一定的影響。已有研究表明相互連通的孔道類型能夠提供更為通暢的通氣過程。具有三維立方連通孔道的SBA-1與具有相似孔徑和比表面積而無連通孔道的SBA3相比,SBA-1具有更快的藥物釋放速率。
另外,研究還表明,相對于其他類型的孔結構籠狀―維結構的孔道能夠提供更高的藥物吸附量以及更緩慢的藥物釋放速率。Kjellman等分別利用有無微孔的SBA-15作為疏水性藥物達沙替尼的載體,并研究了它們的體外釋放行為結果顯示:具有微孔的SBA-15體外釋藥行為更為理想,在初始狀態,藥物釋放速率較高之后則保持在一定的水平范圍。這可能是由于微孔的存在能夠使難溶性藥物以單個分子的形式被限制在孔道中,進而使藥物可以穩定地釋放。然而,當無微孔存在時藥物更容易結晶成穩固的且不易溶的水合物形式從而導致藥物的釋放速率隨著時間的推移而降低。
5、表面官能化
通常情況下藥物分子通過弱的非共價相互作用(如氫鍵、物理吸附和靜電相互作用)與介孔二氧化硅相結合。因此,采用適當的官能團對其進行修飾可以改善藥物的吸附和釋放性能。Mortazavi等用3-氨丙基三乙氧基硅烷改性后的MCM-41作為布洛芬的藥物載體,結果表明:由于改性后的MCM-41與藥物形成了較強的共價鍵,使得藥物釋放速度減緩,從而實現藥物的可控釋放。Bouchoucha等用磷酸酯硅烷對介孔二氧化硅進行表面修飾發現其可以更好地控制帶正電荷藥物的吸附和釋放。
6、殼層厚度
對于中空介孔二氧化硅而言,殼層的厚度也會影響藥物的釋放行為。在相同時間內隨著殼層厚度的減小,藥物的釋放百分量明顯增加,而空心尺寸的變化則對藥物釋放量的影響較小。這主要是由于HMS的殼層越薄,其對藥物擴散的限制能力越弱,藥物的釋放百分量顯著增加。但空心尺寸的變化并不會影響藥物的擴散能力,不同空心尺寸的HMS藥物釋放百分量基本相同。因此,藥物的釋放行為主要受殼層厚度的影響。
綜上所述,在介孔二氧化硅藥物遞送系統中,載體對藥物的吸附和釋放性能是衡量藥物遞送效率的重要指標。藥物的遞送效率主要與介孔二氧化硅的孔徑、孔容、比表面積、孔結構類型及表面官能化有關。孔徑和孔容主要通過空間位阻來影響藥物的吸附與釋放。而比表面積和表面官能化則主要通過增加活性作用位點以及藥物與介孔二氧化硅的相互作用力來增加藥物的吸附量。孔道的結構類型在一定程度上也會影響藥物的吸附和釋放。此外,對于中空介孔二氧化硅而言,其殼層的厚度會影響藥物的擴散能力進而影響藥物的釋放性能。
七、MSNs的藥物釋放
隨著對治療水平要求的提高,人們希望藥物在到達病灶部位前實現“零釋放”,并且不被機體代謝掉,而在病灶部位實行定點釋放。但MSNs在載藥和藥物遞送過程中藥物容易泄漏,納米粒容易聚沉,最終造成給藥劑量不準,達不到實驗效果,并且釋放的藥物可能產生毒副作用。隨著研究的深入,基于環境響應性的藥物控釋逐漸成為研究的熱點。
1、膜包被MSNs緩釋藥物
膜包被MSNs是近些年來開發納米載體的新技術,磷脂作為細胞膜成分具有良好的生物相容性,包被的MSNs具有更好的穩定性,并且能達到緩釋藥物的效果。目前,科學家正探索著用細胞膜包被MSNs,利用不同細胞膜表面的特性發揮更加深遠的作用。通過旋膜法制備磷脂包被的MSNs,在MSNs表面裹有一層致密磷脂,阻止了藥物的泄漏,更是提高了納米粒的生物相容性,MSNs在體內也能夠長循環。Liu等對磷脂包被MSNs作了深入研究,利用MSNs與磷脂表面電性差異,通過靜電作用共孵育制得MSNs。在透射電鏡下可以看到MSNs表面包被著一層約5.5nm厚度的磷脂層。脂包被MSNs防止藥物泄漏并不是唯一的方法。用細胞膜作為運輸載體越來越多的被關注與研究,與磷脂相似的紅細胞膜也可以用來包被MSNs,紅細胞膜包被的MSNs能躲避巨噬細胞的吞噬,使藥物在體內能夠長循環,也能增加樹突狀細胞對納米粒的攝取,引發免疫效應。Xuan等研究巨噬細胞膜包被的MSNs在透射電鏡下可以清晰的看到MSNs外層的巨噬細胞膜結構。納米粒在體內能阻止內皮網狀系統的攝取,促進藥物長循環,膜上的蛋白有靶向腫瘤部位的功能,負載化療藥物的MSNs有效的抑制了腫瘤生長。
2、堵孔MSNs阻止藥物泄露與環境響應性釋放
MSNs表面易修飾性不僅能使藥物靶向到病灶部位,還可以利用修飾上的基團堵住MSNs的介孔,阻止藥物突釋,甚至能利用病灶部位的特殊環境實現藥物的定點釋放。裝載在孔道里的藥物容易從孔道里泄漏出來,而MSNs表面修飾的苯硼酸,再與β-環糊精通過硼酸酯鍵連接,β-環糊精就能堵住MSNs的孔,將藥物封閉在介孔內。苯硼酸酯在酸性或糖溶液中容易水解,通過調節藥物釋放環境中的酸度與糖濃度,可以實現藥物的可控釋放,對于糖尿病與腫瘤的治療有一定的借鑒性。修飾上苯硼酸的MSNs還可以通過中間體功能化多肽(由聚陽離子細胞穿透肽-多聚精氨酸和基質金屬蛋白酶2底物肽兩部分組成)與人體血清白蛋白(HSA)共價連接。HSA密封于MSNs表面,阻止了藥物分子的泄漏。藥物釋放依賴于腫瘤部位過表達的基質金屬蛋白酶2的作用,HSA酶解,從而靶向釋放藥物。通過雙硫鍵接上RGD多肽的載藥MSNs主動靶向腫瘤部位也能起到很大的效果,并能實現谷胱甘肽(GSH)還原敏感性釋放。
結語
MSNs作為藥物遞送載體,以安全性、高載藥量著稱,在生物醫藥領域展現出極大的應用前景。HMSNs的特殊結構對親疏水藥物的共包封,甚至對3種藥物的共包封,將化療與多種抗腫瘤手段聯合,在治療腫瘤方面開辟了新途徑。可降解的MSNs已能成功制備,增加了給藥劑型的安全性,目前對易降解的HMSNs的研究與應用也在不斷加強,不斷優化藥物載體,加強其細分應用,這是需要花費大量時間和精力的大課題。
唐佳民,等:介孔二氧化硅納米粒的研究進展,現代藥物與臨床
崔妍,等:介孔二氧化硅在藥物遞送系統中的研究進展,北京化工大學
郭秀麗,等:功能化介孔二氧化硅復合微球的制備及載藥研究,河南大學
注:圖片非商業用途,存在侵權告知刪除!