中國粉體網訊 目前,已報道的室溫鋰離子電導率接近甚至超過液態電解質水平(10-2 S cm-1)的固態電解質有氧化物電解質和硫化物電解質這兩類材料。然而,氧化物固態電解質受限于其超高的燒結溫度和較差的機械加工性能;硫化物固態電解質則存在電化學窗口較窄,與正極材料兼容性較低,且在潮濕環境下極易分解產生H2S氣體。氧化物和硫化物固態電解質存在的上述問題限制了它們在全固態電池領域的應用。
鹵化物基固態電解質在室溫下的離子電導率能達到10-3 S·cm-1,且理論離子電導率可達10-2 S·cm-1量級。理論模擬結果表明,相比其他固態電解質,鹵化物一般具有較高的氧化還原電位(氯化物>4 V vs.Li/Li+、氟化物>6 V vs.Li/Li+),與高壓正極材料具有更好的兼容性,可以實現在高電壓窗口下的穩定循環。

研究中報道的鹵化物電解質的電化學氧化電位
鹵化物固態電解質的發展過程
鹵化物固態電解質一般是指具有鹵素陰離子框架的離子導體,1930年鹵化鋰(LiX,X=F,Cl,Br,I)已經被證明具有低的鋰離子電導率。基于此,Rao等人在1969年報道了以LiI作為電解質的Li/LiI/I與Li/LiI/AgI/Ag固態鋰電池。然而,該電池由于在正極與電解質界面發生的嚴重極化導致無法反復充放電。
1976年,另一種典型的LiAlCl4鹵化物固態電解質被Weppner等人開發用于電池系統。有趣的是,由于LiAICl4在174℃時顯示出3.5X10-4 S cm-1的離子電導率而首先被用于熱電池。
到1992年,LixTiS2|LiAlCl4|Li1-xCoO2全固態鋰電池被Plichta等人成功組裝,并且在100℃下可以循環超過150次。
1980年代到1990年代,研究者們相繼開發了以二價金屬陽離子(Mg、Pb、Fe、Mn等)為主的尖晶石型鹵化物固態電解質。它們的室溫離子電導率較低,但是在高溫下表現出10-2 S cm-1的高離子電導率。
除了含有二價金屬陽離子的鹵化物固態電解質,含有三價金屬陽離子的鹵化物固態電解質(主要包括Sc、Y和La-Lu的第3族元素,以及Ga和In的第13族元素)也被研究者們持續探究。
Li3InBr6是自1998年以來研究最多的鹵化物固態電解質。這是因為雖然室溫相Li3InBr6的離子電導率較低,但是在高溫發生相變后產生的高溫相具有10-3Scm-1的離子電導率。然而,在-13℃下高溫相又會轉變為低溫相而失去高的離子電導率,故不太適合實際應用。
雖然鹵化物固態電解質的發展時間很長,但是與其同年代發現的其他類型固態電解質材料相比,它較低的離子電導率使得鹵化物固態電解質在過去十幾年中的發展很緩慢。
直到2018年,Asano等人取得了重大發現,即Li3YCl6和Li3YBr6鹵化物固態電解質的室溫離子電導率分別為5.1X10-4Scm-1和1.7X10-3Scm-1。
隨后,其他幾種具有高離子電導率的鹵化物固態電解質也被研究者們發現,如:Li3ErCl6(1.7X10-5 S cm-1~3.3X10-4 S cm-1)、Li3InCl6(8.4X10-4 S cm-1~2.04X10-3 S cm-1)、Li3-xM1-xZrxCl6(M=Y、Er,1.4X10-3 S cm-1)和Li3ErI6(3.9X10-4 Scm-1~6.5X10-4 Scm-1)。
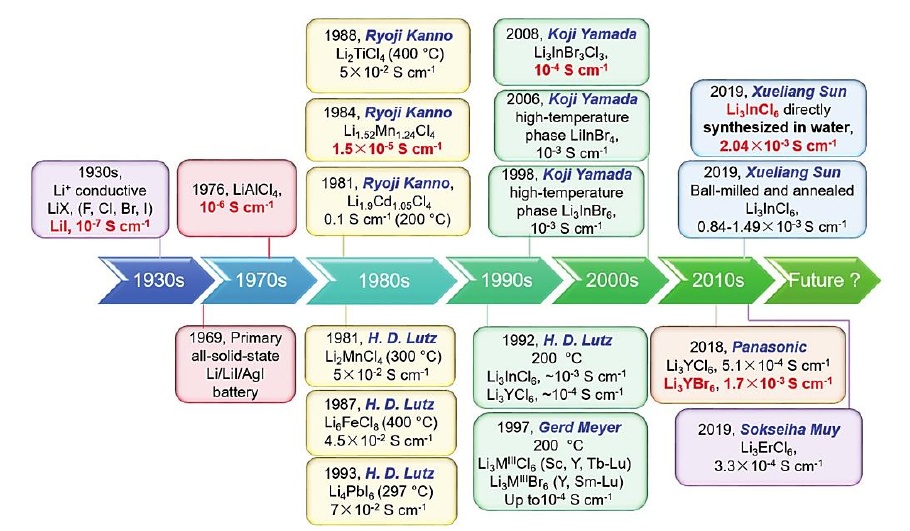
鹵化物固態電解質的主要發展時間點
鹵化物固態電解質的結構
根據M元素的離子價態不同,鹵化物固態電解質可以分為三類:
(1)M元素的離子價態為二價(M=V,Cr,Mn,Zn等);
(2)M元素的離子價態為三價(M=Sc,Y,La-Lu,Al,Ga,In);
(3)M元素的離子價態為四價(M=Zr,Hf)。
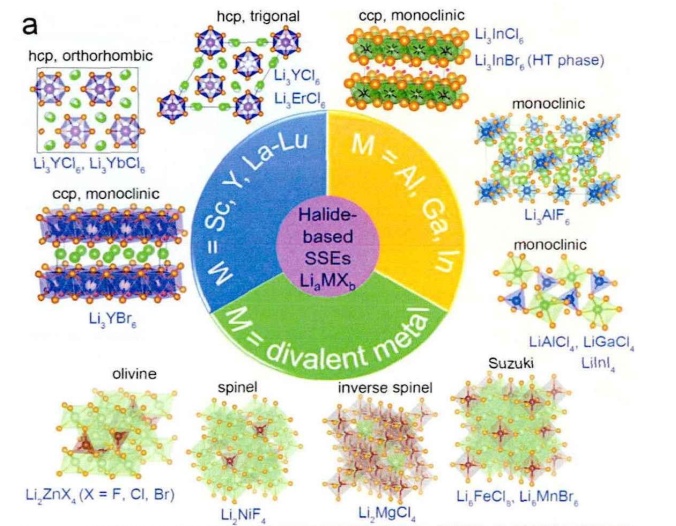
鹵化物LiaMXb(M為金屬元素,X=F、Cl、Br、I)固態電解質的分類
(1)M 元素的離子價態為二價(M=V,Cr,Mn,Zn 等)
此類型固態電解質按照結構主要分為兩類:橄欖石結構和尖晶石結構(正尖晶石、反尖晶石和缺陷型尖晶石)。
在上述兩種結構中,橄欖石結構是唯一具有X-陰離子六方密堆積的結構,其屬于正交晶系,空間群為Pnma,代表物質為Li2ZnCl4,其中所有的Li+占據八面體位置,Zn2+占據四面體位置。橄欖石結構的Li2ZnCl4是一種高溫相結構,由正尖晶石結構的Li2ZnCl4加熱到215℃以上得到。
尖晶石結構的鹵化物固態電解質的結構框架基于X-陰離子的立方密堆積結構,主要形式為Li2MX4(X=Cl,Br),正尖晶石結構中所有的Li+占據八面體位置(Li+與鹵素陰離子呈六配位關系)。反尖晶石結構中,一半的Li+占據四面體位置(與鹵素陰離子呈四配位關系),另一半的Li+和二價陽離子一起占據八面體位置可以表達為(Li)tetr(LiM)octX4。缺陷型尖晶石是指Li2-2xM1+xCl4固溶體。
低溫Li2ZnCl4是一種典型的具有正尖晶石結構的鹵化物固態電解質,空間群為Fd-3m,其中所有的Li+占據著八面體位置,Li+在電解質中通過八面體的共有面以及四面體間隙進行遷移,但是在四面體位的Li+決定了電解質具有高的離子電導率,這解釋了正尖晶石結構的鹵化物固態電解質的離子電導率非常低的原因。
(2)M元素的離子價態為三價(M=Sc,Y,Er,Al,Ga,In)
在Li-M-X體系中,X多為Cl-、Br-、I-。F-由于其較小的離子半徑(133 pm),以及較大的電負性,對鋰離子會產生較大的束縛力,增大離子遷移能壘,不利于鋰離子遷移,如LiF-YF3的室溫離子電導率只有2×10-9 S cm-1,LiF-ScF3的室溫離子電導率僅有~10-6 S cm-1。
在Li-M-X(X=Cl-,Br-,I-)型固態電解質中,主要有三種結構:
1)三方晶系結構,空間群為P-3m1,包括Li3YCl6、Li3ErCl6和Li3ErI6;
2)正交晶系結構,空間群為Pnma,包括Li3YbCl6;
3)單斜晶系,空間群為C2/m,包括Li3ScCl6、Li3InCl6和Li3YBr6。

Li3lnCl6固態電解質結構示意圖
3)M元素的離子價態為四價(M=Zr,Hf)
此類型鹵化物固態電解質目前為止報道得較少,在2020年,Nazar等人通過Zr4+取代Y3+得到Li3-xY1-xZrxCl6,但是Nazar等只研究到x=0.8。
2021年,Kwak等將取代量增大到x=1得到Li2ZrCl6,通過簡單機械球磨得到的Li2ZrCl6呈三方結構,離子電導率為4.0×10-4 S cm-1,將球磨得到的樣品在260℃下退火后,得到的Li2ZrCl6呈單斜結構,離子電導率大幅度降。
Kwak等認為三方結構中存在的M2-M3位點無序是其離子電導率遠高于單斜結構的重要內因之一。Wang等人進一步研究了Li2ZrCl6兩種結構中的離子電導差異,采用鍵價位能理論研究了兩種結構中的離子遷移路徑和遷移能壘,三方相結構中的遷移能壘顯著小于單斜結構,因而三方結構的Li2ZrCl6具有更高的離子電導率。
鹵化物固態電解質的性能優勢
相比目前研究中報道的硫化物基固態電解質,鹵化物電解質的優勢在于其可預見的價格優勢及其極高的氧化穩定性。固態離子導電劑中,硫化物電解質具有最高的電導率,但是其主要原料Li2S的價格價格遠高于LiCl的價格,此外鹵化物制備過程中不會產生H2S等有毒氣體,不需要嚴格的惰性氣氛,理論上只需要在足夠干燥的氛圍下就不會有副產物的生成,水系合成策略也非常適配工業大規模的生產環境。
目前研究中鹵化物由于使用了大量的貴金屬稀土元素(In、Sc、Y等),其價格及元素豐度都有所欠缺,然而近年的鹵化物電解質研究中廣泛使用的Zr元素具有非常可期的價格優勢前景。已有研究證實的Fe3+摻雜的Li2ZrCl6同時具備10−3 S·cm−1數量級的電導率和高的氧化穩定性,與三元正極也實現了較穩定的電池循環。
此外,研究中普遍確認并證實了鹵化物具有適合匹配高壓正極的寬穩定性窗口和界面兼容性,相對于同樣具有正極穩定性的氧化物電解質,鹵化物又兼顧了較好的力學性能、普遍達到10-3 S·cm−1。
鹵化物電解質的固有優勢在于兼顧了高氧化穩定性和寬電化學窗口的同時兼顧了離子電導率,因此有望作為固態電池應用中的一項重要的正極改善和應用策略。目前鹵化物電解質的研究進展較快,其離子電導率、正極材料兼容性、空氣/潮濕環境穩定性等問題還有待進一步改善,但其低成本、環境友好,相比其他電解質具有更為優異的高電壓正極穩定性,相對較高的鋰離子電導率等特性適合作為一項獨特的正極側的電解質策略推動全固態電池走向實用化。
鹵化物固態電解質的應用進展
鹵化物固態電解質在提升正極電壓窗口、降低界面阻抗、改善電解質抗氧化性上具有優異的性能,因而在構筑高能量密度的全固態鋰電池中具有重要的應用價值和實用前景。
在全固態鋰電池結構組成中,鹵化物固態電解質一般作為“鋰離子添加劑”加入到正極混料中或直接作為電解質層來隔絕正極混料中活性物質與不穩定固態電解質層之間的副反應。
鹵化物電解質尤其是氟化物電解質在提升高電壓窗口及高電壓長循環穩定性上具有優勢。
鹵化物電解質與大部分氧化物和三元正極材料接觸時都具有良好的化學/電化學穩定性,并且電解質本身具有較寬的電化學窗口。除了作為“鋰離子添加劑”加入到正極混料中外,鹵化物電解質還可以通過ALD原子沉積法均勻地包覆在正極活性材料表面,以達到隔絕與硫化物電解質的副反應從而實現穩定正極結構的作用,如LiAlF4包覆的LiNi0.8Co0.1Mn0.1O2等。
鹵化物固態電解質的合成路徑
鹵化物的合成是晶體結構重組的化學反應過程,早期實驗中金屬鹵化物多采用液相溶劑結晶和固相混合燒結等方法。近年來,隨著高能球磨結合燒結工藝在固態電解質制備中應用的興起,硫化物電解質、氧化物電解質及鹵化物電解質等均有采用該合成工藝制備的報道。在鹵化物電解質制備方面,從Asano等成功制備高室溫電導率的Li3YBr6與Li3YCl6電解質開始,球磨工藝成為研究中鹵化物電解質合成的主流工藝。
當前,鹵化物固態電解質的合成主要采用機械混合球磨和高溫燒結路徑,采用其他的合成方法,如液相合成、氣相沉積等,報道的相對較少。在實際的固態電池應用中,鹵化物電解質的粒徑、微觀形貌及力學性質等將對固態電池的性能產生巨大的影響,因而研究鹵化物電解質相關的合成途徑與制備工藝對其實用化發展具有重要意義。
鹵化物固態電解質離子電導率的提升
盡管2018年Asano等人合成出室溫離子電導率可達10-4 S cm-1的鹵化物固態電解質,但是相對于硫化物固態電解質和有機液態電解質10-2 S cm-1的離子電導率,仍有一定的差距,亟需人們探索相應的策略去制備具有更高離子電導率的鹵化物固態電解質。
鹵化物固態電解質一般是由鹵素陰離子組成結構框架,鋰離子和金屬陽離子M一般位于由鹵素陰離子組成的八面體中心,在所有的含鋰八面體中,鋰位均未被完全占據,其中部分為空位,這些空位被認為是鹵化物固態電解質具有10-4 S cm-1量級室溫離子電導率的原因之一,這為研究者探索如何提升鹵化物固態電解質的離子電導率提供了思路。摻雜改性是最常見的研究手段之一,摻雜元素的離子半徑和離子價態影響著電解質材料的晶格常數和離子電導率。
(1)摻雜改性提升鹵化物固態電解質的離子電導率
在氧化物固態電解質和硫化物固態電解質中,摻雜改性的手段非常常見,通過特定元素的摻雜,可以對電解質某一方面性質進行改善,也可能同時對某幾方面性質同時改善。
基于鹵化物固態電解質中空位的重要作用,Nazar等使用熔融鹽的制備方法向Li3YCl6中摻雜Zr4+得到Li3-xY1-xZrxCl6,Zr4+摻雜向Li3YCl6結構中引入新的空位,同時隨著Zr4+摻雜量的增加,Li3YCl6的結構由相Ⅰ(三方結構,P-3m1)經歷相Ⅱ(正交結構,Pnma)向相Ⅲ(正交結構,Pnma)轉變,相Ⅲ中的YCl6八面體相對于相Ⅱ發生了傾斜,且出現部分Li+占據四面體位,Li3-xY1-xZrxCl6在x=0.5時為相Ⅲ,離子電導率達到峰值1.4×10-3 S cm-1,活化能為0.33 eV。Nazar等報道的Zr4+摻雜為后來研究者選擇摻雜元素提供了參考。
(2)合成方法影響鹵化物固態電解質的離子電導率
2018年Asano等合成Li3YCl6時發現機械球磨得到的電解質的離子電導率比退火之后的高,Li3YCl6經過退火結晶度提高時,離子電導率反而降低,Schlem等進一步詳細探索了球磨和退火的制備方法對Li3MCl6(M=Y,Er)的結構和離子電導性能的影響,在Li3MCl6(M=Y,Er)中存在M2-M3位點無序,這種位點無序程度越高,對應離子傳輸通道的瓶頸越大,離子遷移能壘越低,越有利于離子遷移,機械球磨得到的Li3MCl6(M=Y,Er)中的M2-M3無序程度較高,退火之后,這種無序程度降低,解釋了兩種合成方法對離子電導率的影響。
此外,新近研究證實水溶劑制備的Li3InCl6具有優異的離子導電性能和電化學性能,但是這種合成路徑是否具有普適性,是否適合所有組成的鹵化物固態電解質還有待進一步的驗證。
鹵化物電解質與電極材料的兼容性
在正極活性材料兼容性方面,當前鹵化物電解質更多的是與高電壓正極材料在常規電化學窗口下工作。提高電解質的高電壓穩定性,擴寬工作電壓窗口對于高電壓和高容量層狀正極材料性能的發揮至關重要,但是鹵化物電解質在高電壓窗口下的電化學表現研究較少。
在負極材料兼容性方面,鋰金屬負極的高理論比容量和低工作電壓使其成為發揮全固態鋰電池高能量密度的關鍵一環。但是當前大部分鹵化物電解質還無法和純的鋰金屬負極甚至鋰銦合金負極等兼容。
采用F摻雜等策略使電解質與鋰金屬間形成更致密的中間層,不僅能改善其與鋰金屬負極的兼容性還能提高電解質的電化學穩定性窗口和抗氧化性窗口,為鹵化物電解質的穩定性/兼容性改善做了探索性的研究。然而鹵化物電解質的負極不穩定性是由于過渡金屬離子導致的本征缺陷,因此需要盡量采用類似多電解質層的策略來避免鹵化物與負極的直接接觸。
小結
作為一類新興的無機固態電解質材料,鹵化物電解質存在的一些問題有望在未來幾年得到改善,最終使其成為最有前景的固態電解質之一。
參考資料:
[1]陳帥、余創、謝佳等:鹵化物固態電解質研究進展,華中科技大學
[2]王凱:基于第四副族金屬鹵化物的全固態鋰電池,中國科學技術大學
[3]許曉偉:鹵化物固態電解質的性能優化與界面改性研究,華中科技大學
(中國粉體網編輯整理/平安)
注:圖片非商業用途,存在侵權告知刪除!