
北京海岸鴻蒙標準物質技術有限責任公司
 白金會員
白金會員 已認證
已認證

北京海岸鴻蒙標準物質技術有限責任公司
 白金會員
白金會員 已認證
已認證
可見異物是導致注射產品召回的十大原因之一。美國食品藥品管理局(FDA)每年都會在其官方網站上公布因可見異物問題而召回的藥品事件。在我國,注射劑的上市質量抽檢中也經常發現可見異物問題。
在注射劑和滴眼劑等藥品中,如果存在可見異物,不僅會對藥品的質量產生不利影響,也會影響其在臨床使用中的有效性和安全性。特別是對于注射劑,一旦可見異物進入血管,可能會引發微循環障礙,導致靜脈血管炎、血栓、變態反應等嚴重后果。此外,可見異物還可能攜帶細菌微生物,引發熱原反應。更嚴重的是,血液中的纖維蛋白可能會附著在可見異物上形成血栓,當這些血栓流經心腦血管時,可能會對患者的健康造成更為嚴重的危害。
在中國,國家藥品監督管理局(NMPA)通過發布一系列指導原則和技術規范來加強對注射劑中可見異物的管理。比如,《中華人民共和國藥典》明確規定了不同類型藥物和不同給藥途徑下可見異物的標準。此外,中國醫藥質量管理協會也積極推動《注射劑、滴眼劑等可見異物課題研究》,旨在制定統一的團體標準和指導原則。
隨著科學技術的進步,自動化檢測設備如顯微鏡觀察、拉曼光譜、激光誘導擊穿光譜等被廣泛應用于可見異物的識別與分析。然而,盡管技術手段日益先進,制藥企業在實際生產過程中仍然面臨著諸多挑戰,包括如何有效地從源頭上減少異物的產生以及如何準確地進行風險評估等問題。
注射劑可見異物的來源及控制
所有注射藥品在生產過程中都可能受到固體 顆粒物質的污染,包括纖維、灰塵、橡膠和硅酮等。這些顆粒物質對患者的影響取決于多種因素, 但考慮到每年有大量患者接受注射藥品,因此降低注射藥品中的顆粒物污染至關重要。
伴隨著全生命周期管理概念的建立,即覆蓋產品生命周期的質量控制,從產品開發階段,就應考慮如何減少或消除可見顆粒的產生,比如原料的選擇、生產工藝的優化以及包裝材料的設計等多個方面。在制造過程中,應實施嚴格的質量控制措施,確保生產環境的清潔度,以及設備的維護和保養,從而避免顆粒的引入。同時,對每一批次的產品都應進行嚴格的檢查,確保符合質量標準。質量風險管理計劃也是關鍵的一環。通過識別、評估和控制與可見顆粒污染相關的風險,可以更有效地預防問題的發生。當發現顆粒污染時,應立即進行調查,找出原因,并采取適當的糾正措施,以防止問題再次發生。因此通過實施可見顆粒控制的全生命周期方法和質量風險管理計劃,生產者可以確保注射用藥物產品的質量和安全性。
全自動燈檢機可以檢測外觀缺陷、內容物缺陷、容器完整性等,同時也存在一些缺點,如氣泡很可能會被相機識別為異物,將合格品誤剔。同時產品中的透明異物無論采用人工檢驗或是全自動設備檢驗,都有一定的漏檢率。西林瓶肩部、頸部或側壁的液滴對檢測的干擾,使得膠塞缺陷無法得到檢驗;安瓿瓶瓶肩和頭部藥液掛壁對檢測的干擾,使得部分用戶只得關閉側壁檢驗工位。可見異物漂浮在藥液面上,與藥液的液位線完全重疊,燈檢機無法識別。這樣就導致了燈檢過程中有一定的漏檢率,因此,對全自動燈檢機的驗證也是比較重要的。
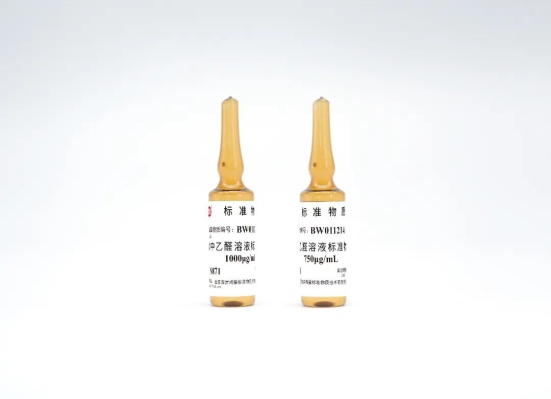
定義: 可見異物標準物質是經過認證的材料,其特性已被充分確定并被廣泛接受作為參考標準。這些標準物質用于校準檢測儀器、驗證分析方法的有效性,以及在藥品質量控制中確保檢測結果的準確性和一致性
校準檢測儀器:
可見異物標準物質用于校準各種檢測儀器,如顯微鏡、光散射儀等,確保這些儀器能夠準確檢測出藥品中的可見異物。
驗證分析方法:
在開發和驗證新的檢測方法時,可見異物標準物質用于評估方法的靈敏度、特異性、線性范圍和定量限等關鍵指標,確保檢測方法能夠準確地檢出并分類不同類型的可見異物。
藥品質量控制:
在藥品生產過程中,可見異物標準物質用于監控和控制產品質量。通過定期檢測,可以及時發現生產過程中的污染問題,采取有效措施進行改進,確保藥品質量符合要求
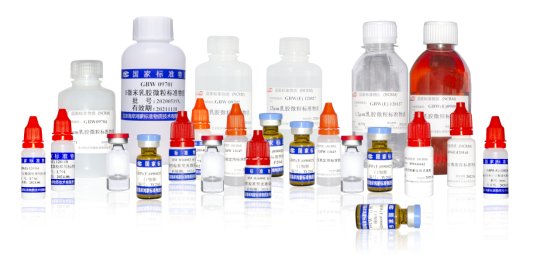
鴻蒙標準物質憑借卓越的技術實力,在微米、納米系列粒度標準物質領域躋身世界水平。公司目前共有200余種顆粒標準物質,其中PM2.5、三聚氰胺、可見異物等百余種標準物質的成功研制,有效解決了國內相關領域的迫切需求。
鴻蒙顆粒產品包括顆粒標準物質和功能微粒兩大類,共有3000多種產品,涵蓋顆粒尺寸從30納米到2000微米,涉及聚苯乙烯、二氧化硅、金屬、膠體金和多元瓊脂糖等不同材質以及彩色微粒、熒光微粒、磁性微粒等不同功能的微粒產品。
最新動態
更多



虛擬號將在 秒后失效
使用微信掃碼撥號